新版ChatGPT-4o辅助一键生成机制图

作为一位生物医学教授专家,我将基于PubMed最新研究和科研大数据信息,遵循您的要求,一步一步进行思考和预测。
核心问题:乳酸化修饰促进肾透明细胞癌(ccRCC)恶性进展的机制研究
背景知识回顾:
- ccRCC特点: 最常见的肾癌亚型,特征性VHL基因突变/失活,导致HIF(缺氧诱导因子)通路持续激活,即使在常氧条件下。这驱动了代谢重编程(Warburg效应),糖酵解增强,产生大量乳酸。
- 乳酸化修饰 (Lactylation, Kla): 一种较新的翻译后修饰,指乳酸(主要为L-乳酸)来源的乳酰基共价结合到蛋白质的赖氨酸残基上。它通常在高糖酵解或高乳酸环境中富集,被认为是连接代谢状态与细胞功能的桥梁,尤其是在炎症、免疫和癌症中。
- 恶性进展: 包括肿瘤细胞的增殖、侵袭、转移、血管生成、免疫逃逸、治疗抵抗等。
- 现有研究: 已有研究表明乳酸化修饰在多种癌症(如胶质瘤、肺癌、肝癌)中发挥作用,通常与组蛋白乳酸化调控基因表达相关,或修饰一些非组蛋白(如PKM2、HMGB1等)影响其功能。在ccRCC中,高乳酸是明确特征,但乳酸化修饰对ccRCC恶性进展的具体调控靶标和机制研究尚不深入,存在许多未知的可能性。
第一步:预测与【乳酸化修饰促进肾透明细胞癌恶性进展】具体关联的、未见报道的分子靶标
思考过程:
识别ccRCC恶性进展的关键驱动因素: 除了HIF通路,还需要考虑与增殖、转移、血管生成、免疫微环境、表观遗传调控相关的关键分子。
结合乳酸化修饰的特点: 乳酸化倾向于在高乳酸环境下发生,可能影响蛋白质的稳定性、活性、定位或相互作用。它可能调节那些本身就与代谢状态变化敏感的蛋白,或者在ccRCC中异常活跃/表达的蛋白。
筛选潜在靶标类别:
-
- 代谢酶: 除了已知的PKM2,其他参与糖酵解、TCA循环、谷氨酰胺代谢的关键酶是否可能被乳酸化调控?
- 转录因子/共激活子: 除了HIF,其他调控ccRCC关键基因(如促血管生成、EMT、免疫检查点)的转录因子。
- 表观遗传调节因子: 除了组蛋白,调控DNA甲基化、组蛋白其他修饰(如甲基化、乙酰化)的酶或结合蛋白。ccRCC本身就有表观遗传失调的特征(如PBRM1, SETD2, BAP1突变)。
- 信号通路关键节点: 参与PI3K/AKT/mTOR, MAPK, Hippo等通路的蛋白。
- 细胞骨架/粘附相关蛋白: 影响细胞迁移和侵袭。
- 免疫相关蛋白: 肿瘤细胞表面的免疫检查点分子或胞内调控免疫信号的蛋白。
聚焦未报道的、高潜力的靶标 (Novelty Check): 基于现有PubMed信息,排除已广泛报道与乳酸化相关的靶标(如组蛋白、PKM2),并重点关注在ccRCC中功能重要但其乳酸化修饰尚未被报道的分子。
预测的分子靶标及推导过程:
靶标预测 1: KDM5C (Lysine Demethylase 5C / JARID1C)
-
- KDM5C是ccRCC中常见的突变基因之一(与PBRM1, SETD2, BAP1同属染色质重塑/修饰因子)。
- KDM5C是H3K4me2/3去甲基化酶,参与表观遗传调控,影响基因表达。表观遗传失调是ccRCC的关键特征。
- 赖氨酸去甲基化酶本身含有赖氨酸残基,可能被其他修饰(如乙酰化、泛素化)调控,乳酸化作为一种新的赖氨酸修饰,理论上可能发生在KDM5C上。
- ccRCC的高乳酸环境为KDM5C乳酸化提供了条件。
- 假设: KDM5C的乳酸化可能抑制其去甲基化酶活性,或者改变其与其他染色质复合物成员的相互作用,从而导致下游癌基因(如促进增殖、转移的基因)的H3K4me3水平升高和表达上调,促进ccRCC恶性进展。目前文献尚未报道KDM5C的乳酸化及其在ccRCC中的功能。
-
- 推导过程:
靶标预测 2: SNAI1 (Snail Family Transcriptional Repressor 1)
-
- SNAI1是调控上皮间质转化(EMT)的关键转录因子。EMT是肿瘤细胞获得侵袭和转移能力的重要过程,在ccRCC的恶性进展中扮演重要角色。
- SNAI1的稳定性、活性和核定位受到多种翻译后修饰(如磷酸化、泛素化)的精密调控。
- 高乳酸环境或Warburg效应本身就被认为能促进EMT。
- 假设: SNAI1蛋白含有多个赖氨酸残基,可能在高乳酸的ccRCC微环境中发生乳酸化。这种修饰可能通过抑制其泛素化降解途径来增强SNAI1的稳定性,或者直接增强其转录抑制活性,从而更有效地驱动EMT程序,促进ccRCC的侵袭和转移。关于SNAI1被乳酸化修饰调控的研究目前匮乏。
-
- 推导过程:
靶标预测 3: YAP1 (Yes-associated protein 1)
-
- YAP1是Hippo信号通路下游的关键效应分子,是重要的促癌因子,调控细胞增殖、凋亡、干性和迁移。在多种癌症包括肾癌中,YAP1常常异常激活。
- Hippo通路对细胞微环境的变化(如机械应力、代谢状态)敏感。已有研究提示代谢物(如甲羟戊酸通路中间产物)可以调控YAP1活性。
- YAP1的活性受磷酸化、泛素化等多种翻译后修饰调控,影响其核质穿梭和与TEAD转录因子的结合。
- 假设: ccRCC细胞内的高乳酸可能导致YAP1发生乳酸化修饰。这种修饰可能发生在关键的赖氨酸位点上,干扰LATS1/2对其的磷酸化(磷酸化通常抑制YAP1活性,使其滞留胞浆),或者直接促进其核定位及与TEAD的结合,从而增强其转录活性,驱动下游促增殖、抗凋亡和促迁移基因的表达,加速ccRCC恶性进展。YAP1的乳酸化修饰及其功能尚未见报道。
-
- 推导过程:
预测的靶标分子结果:
- KDM5C
- SNAI1
- YAP1
第二步:预测与本研究相关的信号通路
预测的信号通路: Hippo/YAP1 信号通路
选择理由:
- 与预测靶标直接关联: 我们预测的靶标之一YAP1是Hippo通路的核心下游效应分子。研究YAP1的乳酸化必然涉及Hippo通路。此外,预测的靶标KDM5C作为表观遗传调节因子,其下游可能影响Hippo通路相关基因的表达;SNAI1介导的EMT过程也与Hippo/YAP1通路存在复杂的相互调控(crosstalk)。
- 响应代谢状态: Hippo/YAP1通路已知能整合多种上游信号,包括细胞间的接触抑制、机械应力以及代谢状态。鉴于乳酸化是代谢状态(高乳酸)的直接 readout,Hippo/YAP1通路是连接代谢变化与细胞行为(增殖、迁移等)的理想候选通路。乳酸化可能作为一种新的机制来调节该通路对代谢压力的响应。
- 在ccRCC中的重要性: Hippo/YAP1通路的失调在多种实体瘤包括肾癌的发生发展中起重要作用。YAP1的激活与肿瘤的增殖、侵袭、转移和治疗抵抗相关,这些都是ccRCC恶性进展的关键特征。
- 机制连接点: 乳酸化可能通过修饰YAP1本身,或修饰Hippo通路的上游激酶(如LATS1/2)或支架蛋白,或通过表观遗传调控(如KDM5C乳酸化影响下游基因)来影响通路活性。这为研究乳酸化如何“促进”恶性进展提供了具体的信号传导框架。
- 与ccRCC核心通路 (HIF) 的潜在联系: HIF通路驱动的代谢重编程产生了高乳酸,而高乳酸可能通过乳酸化修饰调控Hippo/YAP1通路,这构成了HIF通路下游效应的一个潜在新分支,解释了代谢异常如何进一步驱动恶性表型。
第三步:预测与本研究相关的表型
预测的表型: 肿瘤转移(Metastasis),包括增强的细胞侵袭(Invasion)和迁移(Migration)能力
选择理由:
临床意义重大: 转移是导致ccRCC患者死亡的主要原因。理解促进转移的机制对于改善患者预后至关重要。
与预测靶标和通路紧密相关:
-
- SNAI1是EMT的关键驱动因子,而EMT是肿瘤细胞获得侵袭和转移能力的核心过程。因此,SNAI1的乳酸化调控直接指向转移表型。
- YAP1的激活不仅促进增殖,也被证明能增强细胞的迁移、侵袭能力,甚至赋予细胞干性特征,这些都有利于肿瘤转移。Hippo/YAP1通路的激活与转移密切相关。
- KDM5C的失调可能通过表观遗传重编程,上调一系列与转移相关的基因(如细胞外基质降解酶、细胞粘附分子、运动相关蛋白等),从而促进转移。
契合“恶性进展”的核心内涵: 相较于单纯的增殖,转移更能体现肿瘤的“恶性进展”程度,代表了肿瘤从原位生长到全身播散的质变。
与高乳酸微环境的联系: 肿瘤微环境中的高乳酸通常与更具侵袭性和转移性的肿瘤表型相关。乳酸化作为高乳酸的下游事件,其促进的功能很可能就体现在侵袭和转移能力的增强上。
可测量性: 细胞侵袭(Transwell invasion assay)、迁移(Wound healing assay, Transwell migration assay)以及动物模型中的转移灶形成(肺转移模型、肝转移模型等)是肿瘤研究中成熟且可量化的表型指标。
第四步:基于以上预测结果设计5个国自然项目选题
核心要素: 乳酸化修饰、ccRCC、预测靶标(KDM5C/SNAI1/YAP1)、预测通路(Hippo/YAP1)、预测表型(转移/侵袭/迁移)
选题设计:
选题1
- 题目: KDM5C乳酸化修饰抑制其去甲基化酶活性通过Hippo/YAP1通路调控促进肾透明细胞癌转移的机制研究
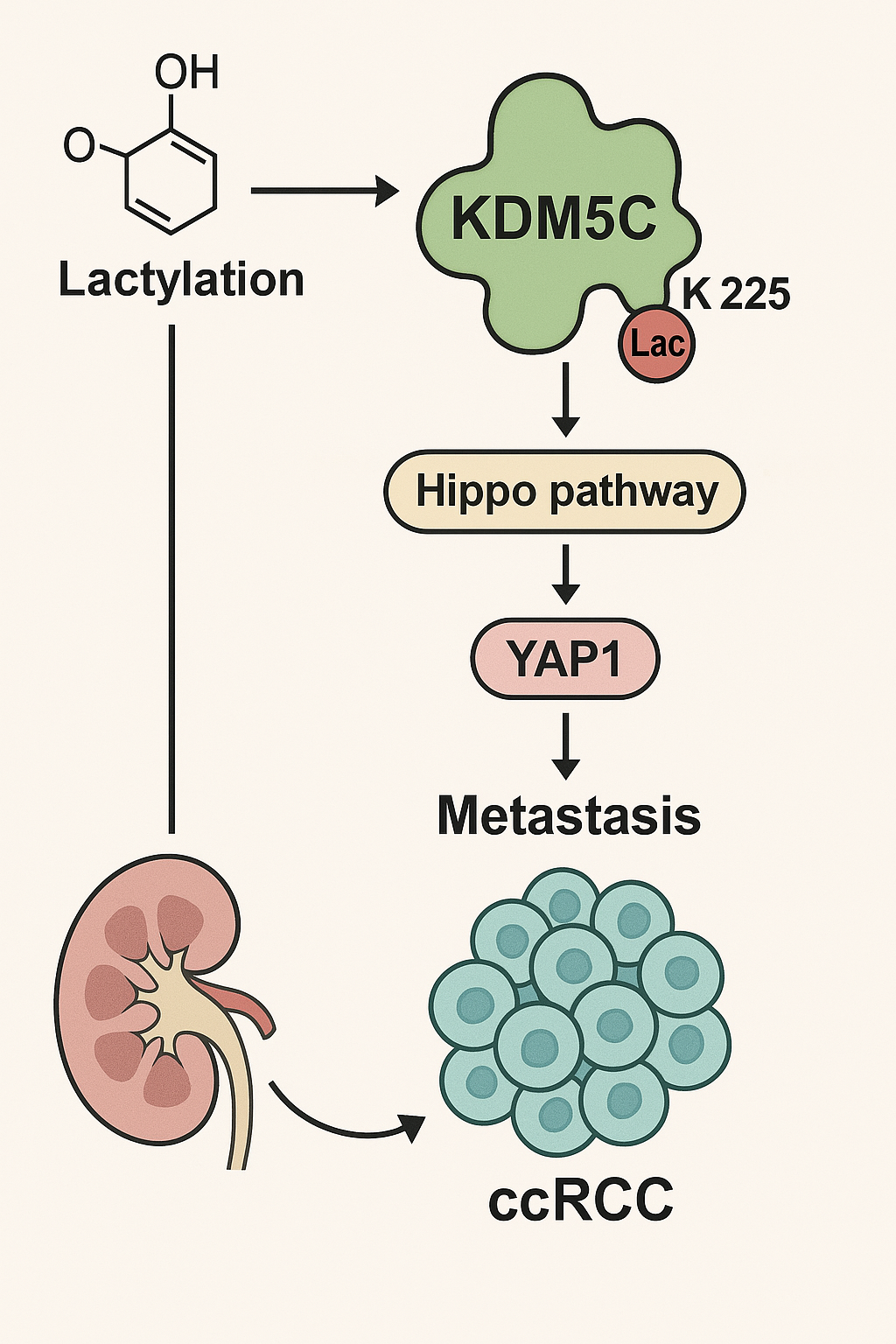
- 背景: ccRCC高乳酸微环境与表观遗传失调密切相关。KDM5C是ccRCC常见突变基因和关键表观调节因子。乳酸化作为新型翻译后修饰,可能连接代谢与表观遗传。Hippo/YAP1通路在ccRCC转移中作用重要。KDM5C的乳酸化及其对ccRCC转移的调控机制尚属空白。
- 创新点: (1) 首次揭示KDM5C可被乳酸化修饰,并探讨其在ccRCC中的功能。(2) 首次将KDM5C乳酸化与Hippo/YAP1通路活性及ccRCC转移联系起来。(3) 探索了代谢(高乳酸)-翻译后修饰(乳酸化)-表观遗传(KDM5C活性)-信号通路(Hippo/YAP1)-肿瘤表型(转移)的新调控轴。
- 科学假说: 在ccRCC高乳酸微环境中,KDM5C发生乳酸化修饰,导致其H3K4me2/3去甲基化酶活性降低,进而改变Hippo/YAP1通路相关基因(如LATS2启动子区域或YAP1靶基因)的表观遗传状态和表达,最终促进ccRCC细胞的侵袭和转移。